アロフィセル注 発売中
再生医療に関する法律
わが国の再生医療に関する法律としては、「再生医療を国民が迅速かつ安全に受けられるようにするための施策の総合的な推進に関する法律」(「再生医療推進法」)、「再生医療等の安全性の確保等に関する法律(「再生医療等安全性確保法」)、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」(「薬機法」)があります。再生医療の実用化に向けて、研究開発や普及を促進する際の国の責務を明記した「再生医療推進法」が2013年に議員立法により成立し、さらに自由診療や臨床研究における再生医療等の安全性の確保等を図るための基準として「再生医療等安全性確保法」が、また再生医療の実用化に対応できるよう再生医療等製品の特性を踏まえた承認・許可制度として薬事法の改正(「薬機法」)がそれぞれ成立しました(図)。
「薬機法」(「改正薬事法」)において再生医療に用いられる製品は、医薬品や医療機器とは別に「再生医療等製品」として定義され、また、迅速に患者が再生医療等製品による治療が受けられるように、条件及び期限付承認制度が導入されました。また、患者への説明と同意を得るように努めることや、使用等に関する記録と保存を行うこと、再生医療等製品による健康被害についても副作用被害救済制度及び感染等被害救済制度の対象とするなど安全対策についても整備されています(表)。
一方、「再生医療等安全性確保法」では、医療機関が医療として提供する再生医療等について安全性を確保するために、実施の手続きや実施する医療機関の基準、細胞を加工する施設の基準などを定めています。この法律では再生医療等は、リスクに応じて3段階に分類され、厚生労働大臣の認定を受けた再生医療等技術や法律の専門家等の有識者からなる合議制の委員会(認定再生医療等委員会・特定認定再生医療等委員会)の審査や厚生労働大臣への計画の提出などの手続きを経て行うこととされています。
■ 図.再生医療に関する法律
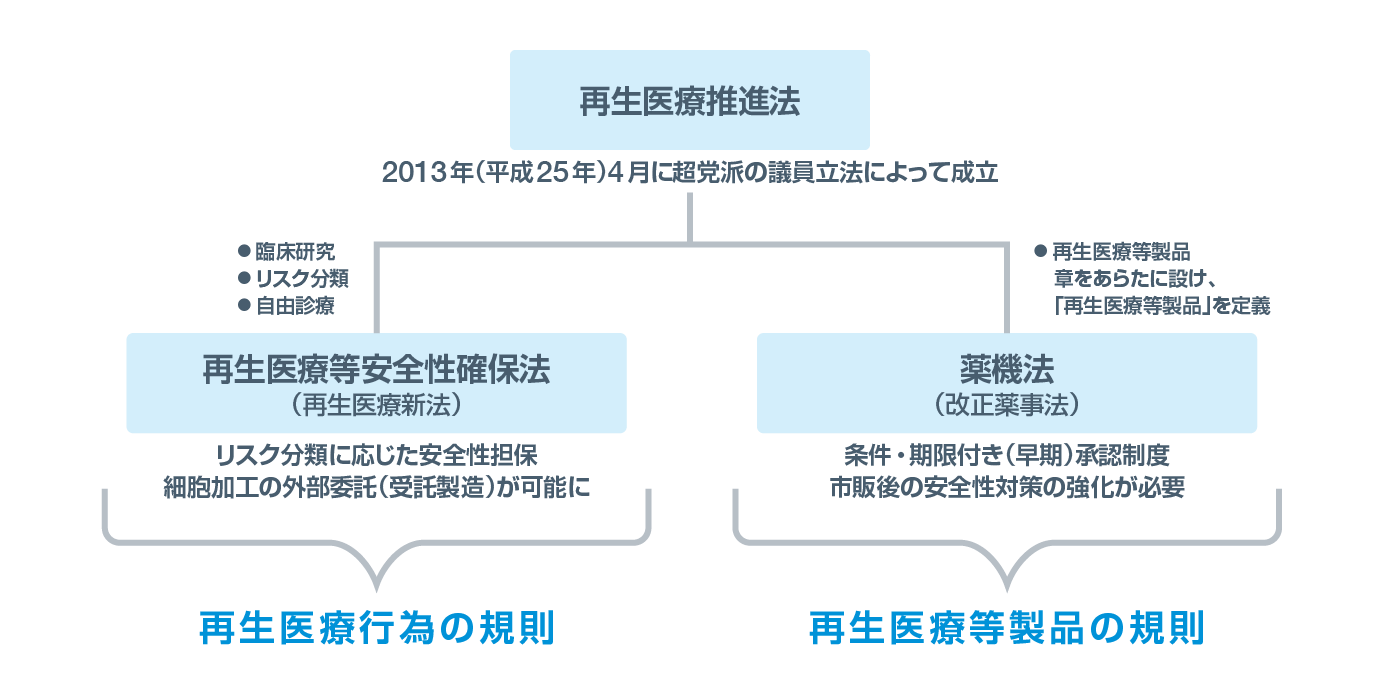
前川 平.: 日本内科学雑誌. 2019; 108(7): 1359-1368.より改変
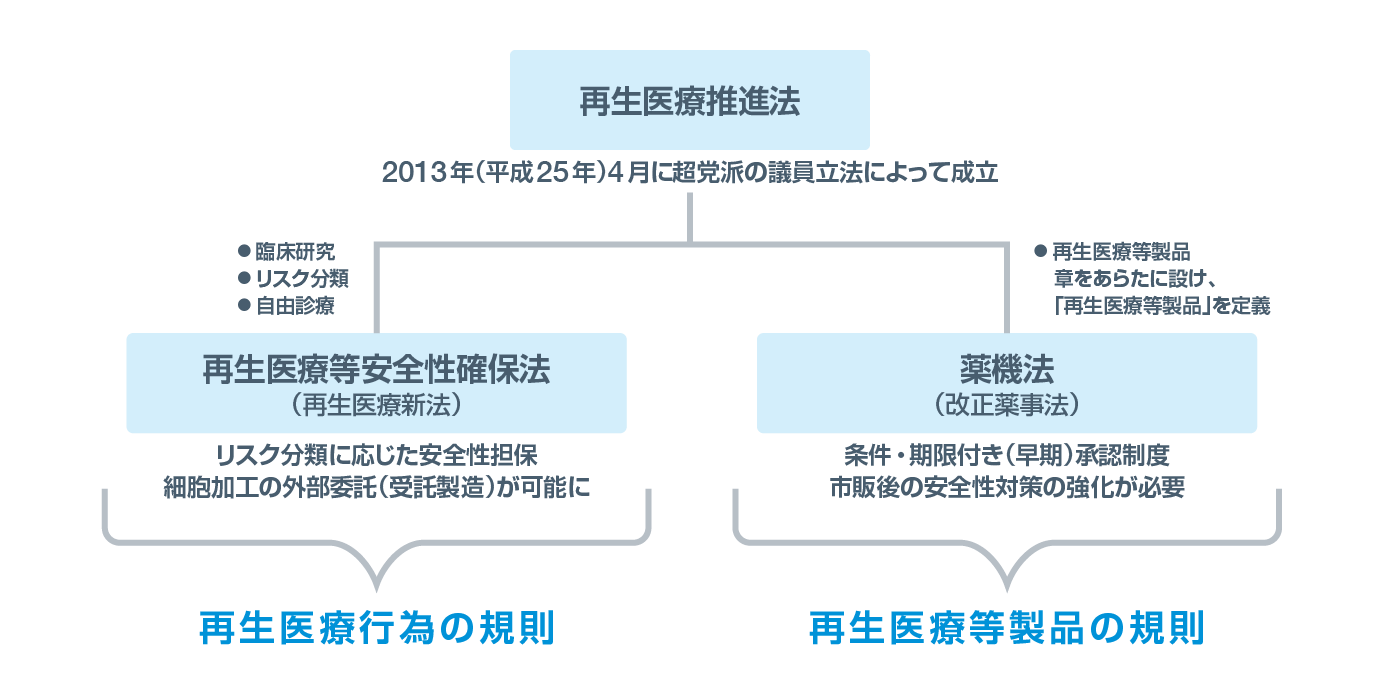
前川 平.: 日本内科学雑誌. 2019; 108(7): 1359-1368.より改変
■ 表.薬機法における再生医療等製品の安全性対策

